Ученые впервые разработали анализ крови, измеряющий количество белка MTBR-tau243. Его количество коррелирует с тяжестью болезни Альцгеймера, а точность теста достигает 92%. В будущем он может использоваться для более индивидуального и эффективного подбора терапии. Исследование опубликовано в Nature Medicine.
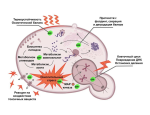
Одной из основных причин возникновения болезни Альцгеймера ученые на данный момент считают накопление белка бета-амилоида. Он образует в нейронах плотные скопления — бляшки. Спустя еще несколько лет бессимптомного развития заболевания в мозге начинают накапливаться тау-белки, что нарушают работу микротрубочек — внутриклеточного «скелета» нейронов. Явные симптомы нейродегенеративного заболевания возникают, когда скопления тау-белков достигают заметного объема и начинают активно распространяться среди нейронов. Несмотря на то, что полноценного лечения для болезни Альцгеймера до сих пор не существует, наиболее эффективны современные препараты лишь на ранних стадиях развития заболевания, которые в большинстве своем проходят бессимптомно. Одним из «золотых стандартов» для диагностики болезни Альцгеймера на ранних стадиях является позитронно-эмиссионная томография мозга (ПЭТ). Тем не менее не всегда у пациентов есть возможность и средства на эту процедуру.
Одни из наиболее доступных, но менее точных способов выявить болезнь Альцгеймера — различные анализы крови. Эти тесты чаще всего используются врачами для пациентов с когнитивными нарушениями. Но у этих методов есть существенный недостаток: они не показывают стадию развития заболевания.
Группа ученых из США уже несколько лет занимается разработкой подобных анализов крови. Ранее они обнаружили, что количество белка MTBR-tau243 в спинномозговой жидкости коррелирует с количеством тау-белков в мозге. Поскольку операция забора спинномозговой жидкости на анализ достаточно дорогостоящая и трудоемкая, ученые решили исследовать, есть ли схожая корреляция между количеством MTBR-tau243 в крови и количеством тау-белков в мозге. Для этого исследователи решили изучить эту корреляцию на двух когортах: когорте добровольцев из Медицинского центра Университета Вашингтона, включавшей 108 человек, и подгруппе из 55 человек из шведской когорты BioFINDER-2. Среди всех пациентов с болезнью Альцгеймера наблюдалась градация в выраженности симптомов заболевания: в выборке были люди как на бессимптомной, так и на поздних ее стадиях. Также стоит отметить, что среди добровольцев были здоровые люди и больные деменцией, что позволило сравнить действенность разработанного анализа крови на разных стадиях заболевания и узнать, будет ли анализ способен отличить болезнь Альцгеймера от здорового состояния и других видов нейродегенеративных заболеваний.
Ученые обнаружили, что уровень MTBR-tau243 в крови помогает предсказать количество тау-белков в мозге с точностью в 92%. Уровень этого белка в крови пациентов с бессимптомным протеканием заболевания был таким же, что и у здоровых людей. При этом количество MTBR-tau243 в крови пациентов со значительными когнитивными ухудшениями было более чем в 200 раз больше, чем у больных с другими типами деменции. Это демонстрирует, что тест не только способен определять стадию заболевания, но и диагностирует лишь болезнь Альцгеймера, а не другие нейродегенеративные заболевания. Благодаря этому свойству анализа крови врачам будет легче понять, связаны ли когнитивные нарушения пациента с болезнью Альцгеймера или нет. Тем не менее, поскольку тау-белки образуются значительно позже первых предвестников заболевания, бета-амилоидных бляшек, первые MTBR-tau243 появляются лишь с ранними симптомами болезни Альцгеймера. Иными словами, тест не способен отличить бессимптомную стадию от здорового организма, поскольку белков, на наличие которых проводится анализ, еще нет в крови в достаточном количестве.
«На ранних стадиях с низким уровнем тау-белков в нейронах антиамилоидная терапия может быть более эффективной, чем на поздних стадиях. Но после начала деменции с высоким содержанием тау белков, анти-тау терапия или один из многих других экспериментальных подходов может быть более эффективным. Как только у нас появится клинически доступный анализ крови для определения стадии заболевания, а также методы лечения, эффективные на разных стадиях болезни, врачи смогут оптимизировать свои планы лечения с учетом конкретных потребностей каждого пациента», — заключает Канта Хори, соавтор статьи, доцент Вашингтонского Университета.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.