Международная группа исследователей изменила геном бактерии, живущей в протоках сальных желез. Теперь она способна синтезировать белок NGAL, который снижает выработку кожного сала. Это поможет лечить акне и другие кожные заболевания. Результаты исследования опубликованы в журнале Nature Biotechnology.
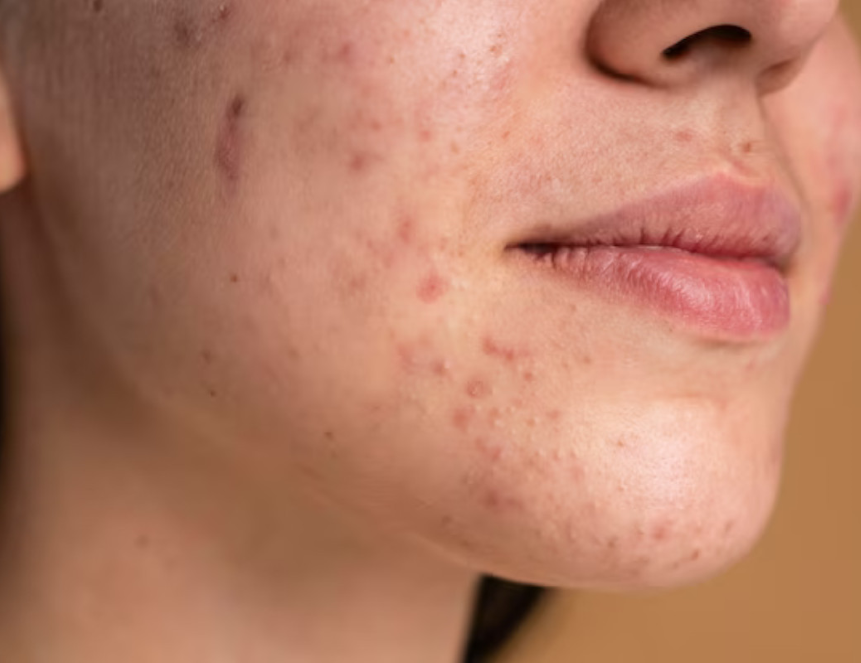
Анке (угревая сыпь) — это распространенное заболевание, вызванное закупоркой и последующим воспалением выводящих протоков сальных желез, связанных с волосяными фолликулами. Оно проявляется по-разному — от невоспаленных «черных точек» на лице до гнойных прыщей по всему телу. Для лечения тяжелых форм акне врачи применяют антибиотики. Они убивают бактерии, которые живут в фолликулах. Также медики используют изотретиноин, вызывающий гибель себоцитов — клеток, вырабатывающих кожное сало.
Проблема в том, что у этих методов лечения есть побочные эффекты. Антибиотики убивают бактерий неизбирательно, поэтому нарушают кожный микробиом, защищающий кожу от болезнетворных микроорганизмов. Токсическое воздействие препаратов на клетки кожи могут вызвать повышенную чувствительность к свету и сильное шелушение. Новым перспективным методом лечения кожных заболеваний может стать использование генетически модифицированных бактерий.
В рамках нового исследования ученые сосредоточились на бактерии Cutibacterium acnes. Она живет внутри устья волосяных фолликулов, практически там, куда из себоцитов выделяется кожное сало. Колонии С. acnes образуют на поверхности протока пленку. Вместе с избыточным ороговением эпидермиса и повышенным выделением кожного сала они приводят к закупорке выводного протока и появлению акне.
«До сих пор C. acnes была трудномодифицируемой бактерией. Было невероятно сложно встроить синтетическую ДНК в ее геном и получить необходимые белки, зашифрованные в вставленном участке», — объясняет Настассья Кнёдлседер из Университета Помпеу Фабра.
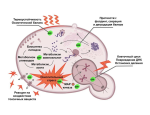
Ученые отредактировали геном C. acnes. Они доставили фрагмент ДНК в ядро и разработали технологию, оберегающую вставленный участок от воздействия регуляторных элементов генома бактерий. Механизм напоминает «троянского коня». Попадая в выводной проток сальной железы, бактерия синтезирует белок NGAL, регулирующий работу себоцитов. Клетки начинают меньше вырабатывать кожное сало, тем самым предотвращая образование прыщей.
Испытания ученые проводили на мышах — единственных организмах, на которых разрешены эксперименты с участием синтетических бактерий. Но кожа мышей не сравнима с человеческой. У них больше волос, эпидермис более рыхлый, содержит меньше липидов. Также у человека и мыши различается механизм потоотделения. Поэтому нужна альтернативная модель, лучше отображающая кожу человека. С этим могут помочь 3D-модели кожи или последующие клинические испытания.
«Мы разработали технологическую платформу, которая открывает возможности для редактирования любых бактерий для лечения множества заболеваний. Сейчас мы сосредоточены на использовании C. acnes для лечения акне, но мы можем доставить генетические схемы для создания синтетических микробов для исследований, связанных с чувствительностью кожи или иммунной модуляцией», — рассказал ведущий автор исследования Марк Гуэль из Университета Помпеу Фабра.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.