Специалисты Отдела функциональной геномики Медико-генетического научного центра имени академика Н. П. Бочкова описали семь пациентов с патогенными вариантами в гене TBCE, которые имеют новый, ранее неизвестный в литературе фенотип. Также ученые установили молекулярные причины его развития. Исследование опубликовано в журнале The Journal of Clinical Endocrinology & Metabolism, сообщается на агрегаторе научной информации InScience.Pro.
Патогенные варианты гена TBCE ранее связывали с тяжелыми заболеваниями: синдромами Санджада — Сакати, Кенни — Кэффи 1-го типа, прогрессирующей энцефалопатией с амиотрофией и атрофией зрительного нерва.
В Отделе функциональной геномики Медико-генетического научного центра имени академика Н. П. Бочкова ученые провели комплексное исследование, в ходе которого совместно с клиническими специалистами выявили семь пациентов с новым, клинически более легким фенотипом. Он проявляется амиотрофией, тестикулярной недостаточностью, умственной отсталостью в легкой форме. Также у пациентов может отмечаться низкий рост.
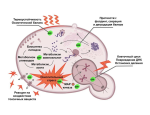
У всех пациентов специалисты выявили один и тот же вариант гена TBCE, который вызывает такие клинические проявления. Уникальность ситуации в том, что выявленный патогенный вариант нарушает сплайсинг, что приводит к сдвигу рамки считывания. Обычно это становится причиной тяжелого течения заболевания, однако у семи пациентов, наоборот, отмечаются более легкие проявления. Потребовался целый ряд научных исследований, чтобы установить причину этого явления.
Специалистам удалось выяснить, что трансляция происходит с альтернативной рамки, поэтому синтезируется белок, способный частично выполнять свои функции. Это является причиной более легких клинических проявлений.
Такое развитие наследственного заболевания удалось описать впервые, в научной литературе не найдено других примеров, при которых установлен подобный молекулярный механизм.
Работа специалистов Отдела функциональной геномики МГНЦ открывает новые возможности для изучения связи генетических вариантов и их клинических проявлений, а также биоинформатического анализа уже описанных заболеваний для более детального их изучения с применением подходов, использованных в этой работе.
«Как правило, сдвиг рамки считывания приводит к полной потере функции гена. Более того, для гена TBCE не описаны случаи полной потери функции обоих копий гена — предположительно, такая ситуация является эмбриолетальной, то есть не совместимой с рождением, однако вопреки этому у наших пациентов мы нашли генетический вариант, который должен полностью ломать работу гена, но с клинически более легким фенотипом. Пришлось применить целый спектр молекулярных методов, для того чтобы установить, что причина данной несостыковки заключается в трансляции с альтернативной рамки, которая компенсировала сдвиг рамки считывания, обусловленный нарушением сплайсинга. Эта работа еще раз показала, насколько важно сегодня детальное изучение связи генотипа и фенотипа, поскольку это позволяет нам выявлять новые клинические формы наследственных заболеваний у человека и лучше понимать, как патогенные генетические варианты реализуются в клинический фенотип. Мы планируем продолжить эту работу и выявить схожие молекулярные механизмы в других генах человека. Работа может помочь лучше понять молекулярные механизмы клинического полиморфизма наследственных заболеваний человека», — рассказал заведующий лабораторией функционального анализа Отдела функциональной геномики Медико-генетического научного центра имени академика Бочкова Петр Спарбер.
Подписывайтесь на InScience.News в социальных сетях: ВКонтакте, Telegram, Одноклассники.